обнаружили мутацию вируса, не реагирующего на анти-тела
тунта, исче интереснее
участок, повышающий инфексионность, на спайковом белке SARS-CoV-2 нацелен на антитела пасиента COVID-19
https://www.biorxiv....3358v1.full.pdf
некоторые из антител против N-концевого домена /NTD/ резко увеличивают способность связывания белка спайков с ACE2 и, таким образом, увеличивают SARS-инфексионность CoV2. К удивлению, мутасионный анализ показал, что все антитела, повышающие инфексионность, распознают конкретный участок на поверхности NTD. в исследовании, антитела против этого участка, повышающего инфексионность, были обнаружены во всех образцах госпитализированных пасиентов с COVID-19. Однако, соотношение антител, повышающих инфексионность, к нейтрализующим антителам у разных пасиентов различалось. антитела против участка, повышающего инфексионность, были обнаружены у 3 из 48 неинфисированных доноров, хотя и на низких уровнях
результаты предполагают, что производство антител против участка, повышающего инфексионность SARS-CoV-2, можно рассматривать, как возможные факторы, усугубляющие COVID-19, и что для безопасной разработки ваксины может потребоваться спайковый белок, не содержащий таких эпитопов антител, особенно для отдельных лиц, с уже существующими усиливающими антителами
и тунта
поверхностные белки вируса sars-cov-2 изменяют экспрессию ключевых цитокинов и хемокинов в клеточных линиях, вызывая интерферон-зависимое воспаление
https://www.biorxiv....2710v1.full.pdf
поверхностные белки SARS-CoV-2 Spike /S/ и Envelope /E/* активируют ключевой путь иммунного сигнального интерферона /IFN/, как в иммунных, так и в эпителиальных клетках, независимо от вирусной инфекции и репликации. Эти белки индуцируют образование реактивных окислительных видов и увеличение специфических IFN-чувствительных цитокинов и хемокинов человека и мыши, аналогично их усилению у пациентов с COVID-19 в критическом состоянии. Индукция передачи сигналов IFN зависит от канонических, но несовместимых медиаторов передачи сигналов воспаления, поскольку активация, индуцированная S, зависит от IRF3, TBK1 и MYD88, тогда как активация E в значительной степени не зависит от MYD88. Кроме того, эти вирусные поверхностные белки, в частности E, индуцировали перибронхиальное воспаление и легочный васкулит на модели мышей. организованные воспалительные инфильтраты зависят от передачи сигналов IFN типа I, особенно в эпителиальных клетках легких. Эти результаты подчеркивают роль поверхностных белков SARS-CoV-2, особенно малоизученного белка E, в управлении клеточно-специфическим воспалением и их потенциале для терапевтического вмешательства.
на закусь - новый тип вируса в Великобритании не может быть обнаружен большинством современных тестов ПЦР
https://twitter.com/...355128818360325
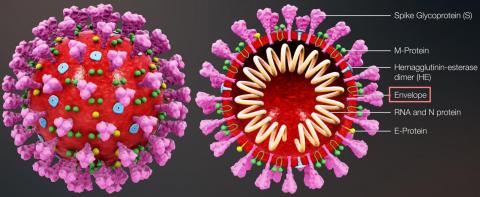
*Модель поперечного сечения большинства представителей группы Beta-CoV B. Однако у вирусных частиц SARS-CoV-2 отсутствует белок Hemagglutinin esterase /HE/
Прикреплённые изображения:

 Войти
Войти Регистрация
Регистрация




 Наверх
Наверх